Groene Chemie (5hv) - Proceschemie
Inleiding
In het onderdeel proceschemie maak je kennis met
- blokschema's
- batch en continu proces
- verschillende typen reactoren
- scheidingsmethoden
- massa- en energiebalans
Het proces
In de chemische industrie wil men in zo’n kort mogelijke tijd zo veel mogelijk van een zo zuiver mogelijk product maken. Dit betekent dat de snelheid een belangrijke factor is.
Bovendien wordt er in de chemische industrie op een grote schaal gewerkt. Het is iets anders dan in een bekerglas wat stoffen bijeenvoegen, ze roeren en op temperatuur brengen en kijk: daar is het product.
Er zijn een aantal gebieden waarbij problemen kunnen optreden, die tijdens of na het proces moeten worden opgelost:
|
Opgave 1
Ethanol, alcohol, kan gemaakt worden door een additiereactie van stoom aan etheen. Dit is een exotherme reactie. De reactie vindt plaats bij 300 °C en 60-70 atm. Als katalysator wordt fosforzuur, dat gehecht is aan vast SiO2, gebruikt. Beantwoord de volgende vragen:
a. Geef de reactievergelijking van deze reactie, waarbij ethanol ontstaat uit etheen en stoom. b. Beredeneer welke van de bovenstaande problemen kunnen optreden bij dit proces.
Opgave 2
Vul de onderstaande tabel in:
Scheidingsmethode Berust op verschil in
Wordt gebruikt bij
Destilleren Kookpunt
Oplossingen
Filtreren
Centrifugeren
Extraheren
Het beroep van een proces ingenieur
Een proces ingenieur in een chemische fabriek heeft als functie om de in kaart gebrachte processen die plaatsvinden in een chemische fabriek te controleren en eventueel aan te passen. Om het proces in kaart te brengen, gebruikt hij blokschema’s.
1. Blokschema
Men brengt de processen die plaatsvinden in een chemische fabriek in kaart in een zogenaamd blokschema, waarbij in ieder blok een stap uit het proces plaatsvindt, b.v. een reactie, scheiding of andere bewerking. Men verbindt de blokken door middel van lijnen, waarbij alle stoffen staan, die een blok binnengaan of uitkomen.
In het algemeen ziet een blokschema als volgt uit:
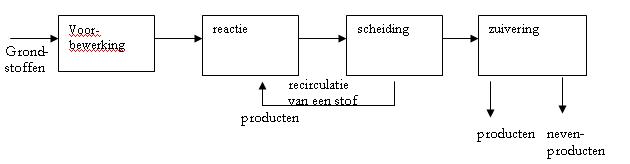 |
In een blokschema blijven de producten dus in de horizontale lijn.
Opgave 3
Per persoon gooien we jaarlijks zo'n 30 kg aan kunststof (plastic) verpakkingen weg. In totaal is dat in Nederland ongeveer 5•108 kg. Al dit afval komt gewoonlijk op een stortplaats of wordt verbrand. De gemiddelde dichtheid van het kunststof is 1,05 kg/dm3.Beantwoord de volgende vragen:
a. Bereken hoeveel ‘kuub’ kunststof (een ‘kuub’ is 1 m3) wordt weggegooid.
De meest milieuvriendelijke manier om kunststof te verwerken is recycling.
b. Wat is recyclen?
Een Nederlands bedrijf wil het kunststofafval omzetten in diesel als brandstof
voor auto’s. Hieronder zie je dit proces in vier stappen afgebeeld.
c. Kun je dit proces tot de groene chemie rekenen? Licht je antwoord toe. d. Geef het proces weer in een blokschema.
Nederlanders brouwen diesel uit afvalplastic:
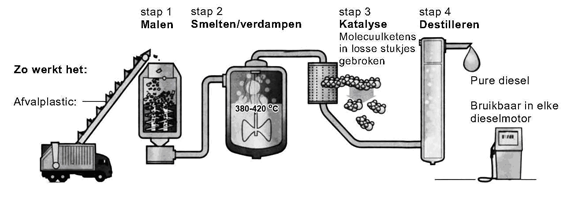
Bron vmbo gt examen NaSk1, 2009-I
Opgave 4
Bij de productie van margarine wordt als grondstof plantaardige olie gebruikt. Deze wordt gewonnen uit zaden. Om zoveel mogelijk olie uit de zaden te halen mengt men de fijn gemalen zaden met hexaan. Na een eerste scheiding verkrijgt men een oplossing van olie in hexaan. Tenslotte worden olie en hexaan van elkaar gescheiden. Het hexaan wordt opnieuw in het proces gebruikt, de olie gaat naar de margarine fabriek. Hieronder is het proces in een blokschema weergegeven.
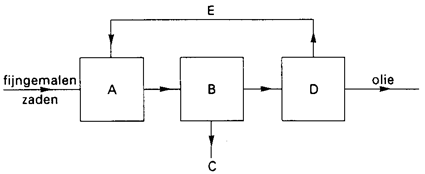
In dit blokschema hoort bij de letters A tot en met E telkens één van de hierna genoemde woorden: afval, destillatie, extractie, filtratie, hexaan.
Geef aan welk woord bij welke letter hoort. Noteer je antwoord als volgt:
Bij A: ...
Bij B: ...
Bij C: ...
Bij D: ...
Bij E: ...
Opgave 5
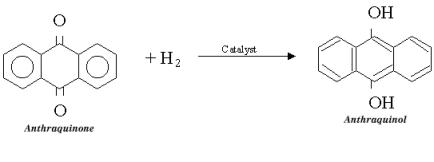
De industriële bereiding van waterstofperoxide uit waterstof en zuurstof vindt plaats in een aantal stappen. Allereerst reageert waterstof in een reactor met de stof anthraquinon tot anthraquinol:
Deze reactie geven we vereenvoudigd weer als H2 + X → H2X
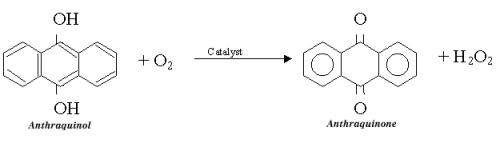
Vervolgens reageert in een andere reactor de stof anthraquinol met zuurstof:
Deze reactie geven we vereenvoudigd weer als H2X + O2 → H2O2 + X
Tenslotte wordt in een scheidingsruimte aan het ontstane mengsel water toegevoegd, H2O2 lost daarbij in water op, de stof anthraquinon (X) niet. De oplossing van H2O2 wordt afgetapt, anthraquinon (X) wordt weer teruggevoerd naar de eerste reactor, om daar opnieuw met H2 te reageren.
Dit proces, dat continu verloopt, kan als volgt schematisch worden weergegeven: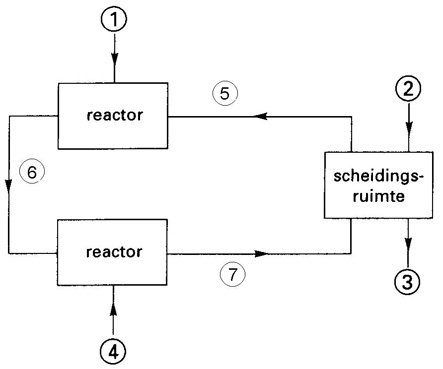
Bij dit proces spelen dus de volgende stoffen een rol: H2, H2O, H2O2, O2, X, H2X.
Geef aan welke stof of stoffen bij de nummers (1), (2), (3), (4), (5), (6) en (7) geplaatst moeten worden. Noteer je antwoord als volgt:
bij (1): ....
bij (2): ....
bij (3): ....
bij (4): ....
bij (5): ....
bij (6): ....
bij (7): ....
Voorbewerking
Er zijn een aantal mogelijkheden voor de bewerking van de uitgangsstoffen.
Hier een aantal voorbeelden:
- De ruwe grondstof moet soms gezuiverd worden van verontreinigingen. Ruwe aardolie bevat meestal te veel zwavel om zo gebruikt te kunnen worden. Men laat de ruwe aardolie reageren met waterstofgas, waarbij de zwavel wordt omgezet in diwaterstofsulfide, dat men makkelijk kan verwijderen.
- Vaste stoffen moeten verpoederd worden om het contactoppervlak te vergroten.
- De uitgangsstoffen moeten worden voorverwarmd.
2. Batchproces en continu proces
Er bestaan twee soorten processen: batchprocessen en continuprocessen.
Bij een batchproces wordt een reactor met de beginstoffen gevuld, vervolgens wordt de reactor op de juiste temperatuur en druk gebracht en reageren de stoffen met elkaar. Na afloop van de reactie wordt de reactor leeggehaald en schoongemaakt.
Vervolgens begint men van voren af aan.
Batchprocessen zijn heel geschikt voor productie op kleine schaal en voor de productie van veel verschillende producten in dezelfde reactor.
Voorbeelden van batchprocessen zijn de productie van geneesmiddelen, kleurstoffen en bier.
Bij een continuproces voert men voortdurend uitgangsstoffen aan en tegelijkertijd voert men ook het product af. De condities in de reactor blijven daarom steeds constant. Bij continuproductie zijn de productiekosten meestal lager dan bij een batchproces, maar een continu proces is minder flexibel dan een batchproces.
Voorbeelden van reacties die via een continuproces worden uitgevoerd zijn de productie van zwavelzuur, salpeterzuur, ammoniak, etheenoxide en ook het kraken van nafta is een continuproces.
Opgave 6
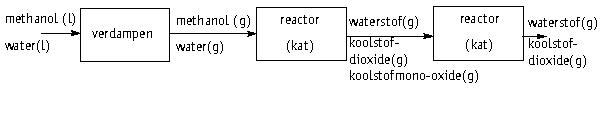
Hierna is het blokschema weergegeven voor de productie van waterstofgas uit methanol, CH3OH, en waterdamp. Er ontstaat als bijproduct koolstofmonooxide.
a. Geef de reactievergelijking van de reactie die plaatsvindt in de eerste reactor.
In de tweede reactor wordt koolstofmonooxide omgezet in koolstofdioxide. Dit gebeurt met behulp van extra waterdamp en niet met behulp van zuurstof.
b. Waarom is het niet wenselijk om hiervoor zuurstof te gebruiken? c. Geef de reactievergelijking van de reactie die optreedt in de tweede reactor. d. Er ontbreekt iets aan dit blokschema. Leg uit wat er ontbreekt. e. Is het mogelijk om aan het blokschema te zien of het handelt om een continu proces of een batchproces? Licht toe.
3. Typen reactoren
Er bestaan verschillende soorten reactoren.
Welke reactor gebruikt wordt bij een proces hangt o.a. af van de volgende factoren:
- homogene of heterogene reacties: wanneer alle uitgangsstoffen en reactieproducten gassen zijn, is er een homogeen systeem en is de keuze voor een continu proces snel gemaakt. Bij heterogene systemen zijn er altijd twee fasen, bij voorbeeld vloeibare fase met een vaste katalysator. Hierbij moet goed gemengd worden om ervoor te zorgen dat de fasen goed in contact komen met elkaar. Dit kan zowel in een batch als continu proces gebeuren.
- De reactiesnelheid van de betrokken reactie. Bij hoge snelheid kan het proces continu verlopen. Bij lage snelheid gebeurt het proces in een batchproces. De verblijftijd van de stoffen in de reactor speelt dus ook een rol.
- De warmte-overdracht in de reactor. De temperatuurverschillen tussen de wand en het midden van de reactor mogen niet te groot zijn.
- Veiligheidsfactoren. Je moet ten alle tijden de omstandigheden, waaronder de reactie plaatsvindt kunnen controleren.
Opgave 7
Bekijk de reactie uit opgave 1(additie van stoom aan etheen) nog een keer.
a. Is het proces, waarbij deze reactie plaatsvindt een homogeen of heterogeen proces? Motiveer je antwoord. b. Beredeneer of je bij dit proces zou kiezen voor een batch of een continu proces.
We beschrijven hieronder een aantal voorbeelden van reactoren.
1. Geroerde tankreactor
Dit is een tank, cilindrisch van vorm, met roerwerk daarin. Geroerde tankreactors kunnen open of gesloten zijn. Er kunnen voorzieningen zijn om te koelen of om te verwarmen. Dit soort reactoren kan zowel voor batch als continuprocessen worden gebruikt. Zie afbeelding 1.
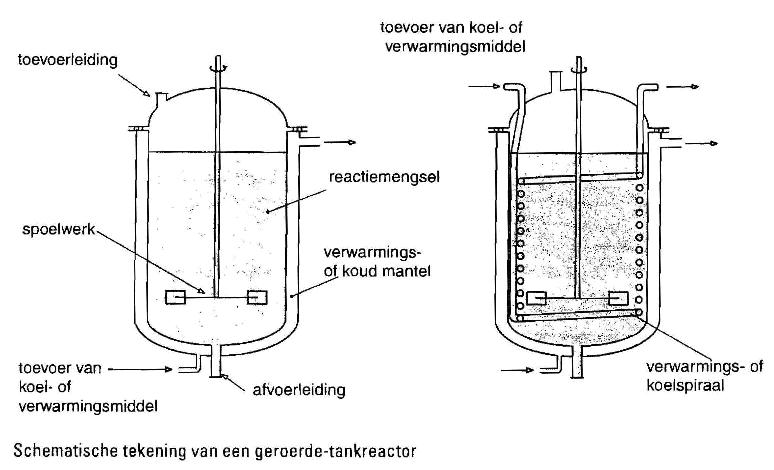 |
Afbeelding 1.
2. Buisreactor
De buisreactor is een reactor in de vorm van een buis. In de wand bevindt zich een verwarmings- of koelmantel. Een buisreactor wordt alleen voor continuprocessen gebruikt. Aan een kant worden de uitgangsstoffen ingebracht en aan de andere kant komen de producten eruit. Terwijl het reactiemengsel door de buis stroomt, reageren de stoffen met elkaar. Zie afbeelding 2.
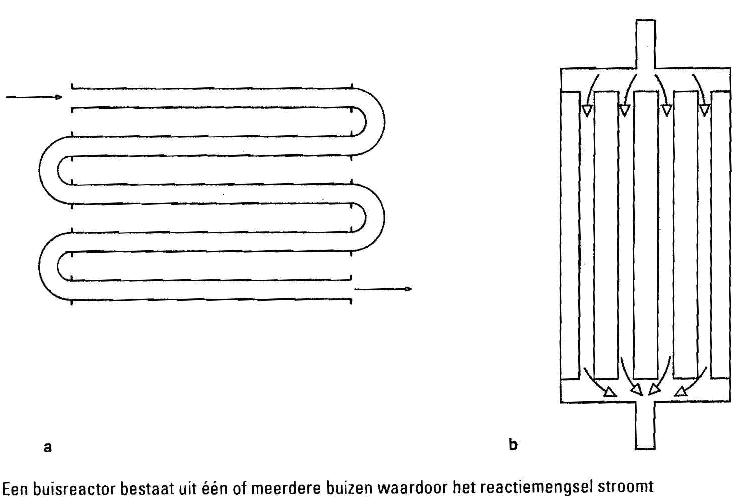 |
Afbeelding 2
3. Fluïd-bedreactor
Een fluïdbedreactor is een cilindrisch vat met onder in een rooster, waardoor de aanvoer van een vloeistof of een gas plaatsvindt. In de reactor bevindt zich vaste stof, die door deze toevoer in beweging wordt gebracht en gehouden. De vaste stof kan zowel een uitgangsstof als een katalysator zijn. Het contact tussen de vaste stof en vloeistof wordt zo bevorderd. Zie afbeelding 3.
Een voorbeeld van toepassing van dit soort reactor is bij het kraken van nafta onder invloed van zeolieten als katalysator. Er is dan veel katalysator in de reactor aanwezig!
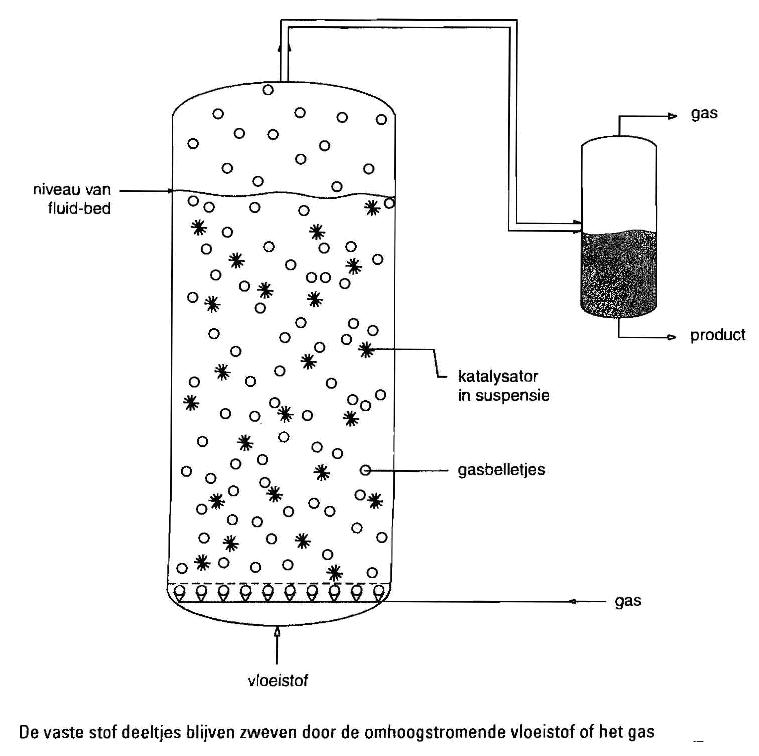 |
Afbeelding 3
Opgave 8
Beredeneer of een fluïdbedreactor hoort bij een batch proces of bij een continu proces.
4. Micro reactor
Men verwacht dat microreactoren dé reactoren van de toekomst zullen zijn.
De term “micro”slaat niet op de buitenkant van de reactor, maar op de binnenkant, waar zich duizenden zeer kleine kanaaltjes bevinden, waardoor de stoffen stromen en reageren. Op deze manier is het proces veel beter beheersbaar dan in één groot vat. Het contact tussen de stoffen is beter en de warmte-overdracht vindt ook beter plaats. Door de kleinere afmetingen is de veiligheid groter dan bij een conventionele reactor. Aan de TU/e bij de faculteit chemische technologie wordt er veel onderzoek gedaan naar het verloop van processen met behulp van micro-reactoren. De foto’s en het schema in tekening 4 zijn afkomstig van de TU/e.
De microreactor is vooral geschikt voor fijnchemische processen. De capaciteit is door de kleine kanaaltjes niet erg groot, maar de capaciteit kan opgevoerd worden door een aantal microreactoren parallel te plaatsen.
 |  | |
| Afbeelding 4a | Afbeelding 4b | |
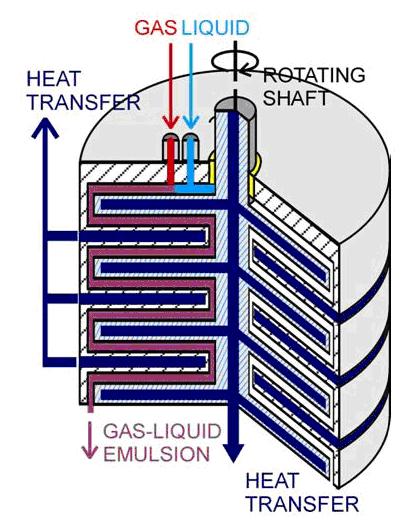 | ||
| Afbeelding 4c | ||
Opgave 9
a. Wanneer de reactie traag is, is het dan beter om een aantal microreactoren in serie of parallel te zetten? Motiveer je antwoord.
Microreactoren bevatten nauwe kanaaltjes. Daardoor komt een klein volume van de stoffen die moeten reageren in contact met een relatief groot wandoppervlak.
b. Leg uit welk voordeel dat heeft, gelet op de reactiesnelheid. c. Leg uit welk voordeel dat heeft, gelet op de energie-aanvoer of -afvoer.
Opgave 10
Schaalverkleining in de scheikundige technologie levert microreactoren met reactiekanalen met een diameter tussen de 10 en 500 micron. Zo komt een klein volume van de reagerende stof met een relatief groot wandopperlvlak in contact. Dat heeft voordelen voor de reactiesnelheid en de warmte-afvoer.
Een toepassing van zo’n microreactor is het omzetten van methanol in waterstof, dat vervolgens in een elektrochemische cel elektrische energie opwekt. Microreactoren en brandstofcel kunnen geïntegreerd worden tot een accu voor bij voorbeeld laptops. Er is een methanol-waterstofomzetter ontwikkeld die bestaat uit drie micro-reactoren. In de eerste vindt de verdamping van de vloeibare brandstof, een mengsel van methanol en water, plaats. In de tweede reactor worden methanol en water onder invloed van een katalysator omgezet in waterstof en koolstofdioxide en een kleine hoeveelheid koolstofmonoöxide, die de brandstof “vergiftigt”. In de laatste micro-reactor oxideert die koolstofmonoöxide onder invloed van een katalysator verder. Uit Technisch weekblad, 17 juni 2005
Bron: Chemie Aktueel
a.
Geef het hele proces voor de productie van waterstofgas uitgaande van methanol en water weer in een blokschema. b. Noteer de reactievergelijkingen van de reacties die optreden in de tweede en derde microreactor. c. Leg uit welke voordelen er zijn voor het gebruiken van microreactoren in plaats van gewone reactoren. Noem er minimaal drie.
4. Scheiden en recirculeren
De mengsels die ontstaan tijdens de chemische reactie worden na afloop gescheiden. Diverse scheidingsmethoden zoals filtreren, indampen en destilleren worden hierbij gebruikt. De uitgangsstoffen die nog niet zijn omgezet, worden teruggeleid in de reactor via een recirculatielus.
Opgave 11
De reactie tussen etheen en stoom, waarbij ethanol wordt gevormd, is een evenwichtsreactie. Men zal dus uit het reactiemengsel het niet-gereageerde etheen terug willen winnen om weer te laten reageren.
a.
Beredeneer hoe je uit het reactiemengsel etheen kunt terugwinnen b. Teken van het proces met de gegevens die je nu kent een blokschema.
Scheidingsmethoden kosten vaak veel energie, zoals bij destilleren, of geven veel extra afval, zoals bij extractie. In het volgende schema worden de scheidingsmethoden herhaald.
| Scheidingsmethode | Principe | Energiekosten | Afvalstromen |
| Filtratie | Deeltjesgrootte | Bij reinigen filters | Residu of filtraat |
| Destilleren / Indampen | Kookpunt | Hoge energiekosten door verhitten | Residu of destillaat |
| Extraheren | Oplosbaarheid | - | Residu of de oplossing |
| Adsorberen | Adsorptievermogen | - | Het adsorptie-materiaal met geadsorbeerde stof |
| Chromatograferen | Adsorptievermogen / oplosbaarheid | - | Loopvloeistof, dragergas |
In de duurzame chemie probeert men dit te voorkomen door nieuwe methodes toe te passen. We zullen er hier twee kort bespreken: selfseparation en membraanscheiding.
Selfseparation:
Wanneer de reactanten met elkaar reageren in de aanwezigheid van een katalysator, moet de katalysator na afloop van de reactie weer verwijderd worden. Hiervoor is vaak een extractie nodig met een oplosmiddel, waarin of de katalysator of de producten oplossen.
Er wordt nu veel onderzoek gedaan naar katalysatoren die wanneer de reactanten beginnen op te raken neerslaan, waardoor ze door bezinking of een eenvoudige filtratie direct weer herwonnen kunnen worden en ook weer gebruikt kunnen worden.
Op deze wijze kan het oplosmiddel worden bespaard.
Er zijn ook katalysatoren die neerslaan door een verandering in temperatuur doordat hun oplosbaarheid in het oplosmiddel zeer sterk afhankelijk is van de temperatuur. In het algemeen lossen vaste stoffen beter in het oplosmiddel op bij hogere temperatuur.
Membraanscheiding:
Membranen zijn kunststoffilters met hele kleine poriën ter grootte van ongeveer 0,1 micrometer. Maar ongeveer 20 % is kunststof, de rest bestaat uit poriën. Kleine moleculen kunnen (in de gasvorm) dit membraan prima passeren. Hieronder is een voorbeeld geschetst voor de toepassing bij de productie van drinkwater uit zeewater.
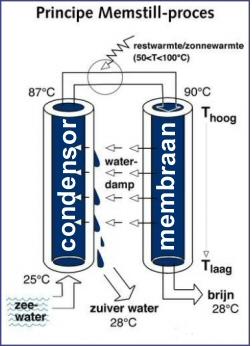 | Schematische weergave van het Memstill proces. Hoewel hier sprake is van buisvormige condensor- en membraancomponenten zijn inmiddels ook plaatvormige componenten in gebruik. De scheiding van vuil zeewater en zuiver (demi-)water vindt plaats in het membraandeel. Daar verdampt water door de poriën van het membraan. Omdat hierbij verdampingswarmte wordt opgenomen, koelt het zoute, geconcentreerde zeewater (brijn) af tot de omgevingstemperatuur. De vrijgekomen waterdamp stroomt naar het condensorgedeelte. De naam zegt het al: de condensor zorgt ervoor dat de waterdamp condenseert zodat het vloeibare zuivere water afgevoerd kan worden. De warmte die bij het condenseren van de waterdamp vrijkomt, wordt in de condensor benut voor het opwarmen van het zeewater (vóórdat dit naar het membraangedeelte stroomt). In het procesontwerp is men uitgegaan van een zeer klein verschil tussen de zeewatertemperatuur na het verlaten van de condensor en vóór het ingaan van het membraandeel. Om het proces te bedrijven hoeft daarom (na een opstartfase waarin het systeem wordt voorverwarmd) slechts 1-3 graden temperatuurverschil overbrugd te worden. Dit maakt het mogelijk om restwarmte of zonnewarmte te benutten, die via een warmtewisselaar (boven in het schema aangegeven) door het systeem wordt opgenomen. |
Bron: Kennislink.nl
Het is ook mogelijk om de reactie en de scheiding tegelijkertijd te laten verlopen, zoals bij het volgende voorbeeld.
Ethaan, C2H6, wordt omgezet in etheen, C2H4, en waterstofgas. Het gebeurt in een buisreactor met een binnenbuis die uit een membraan bestaat. Dit membraan laat alleen waterstofgas door en niet het ethaan en etheen.
Hierdoor is de omzetting bijna 100 % en er is wordt bespaard op dure energieverslindende scheidingsmethoden. Zie afbeelding 5.
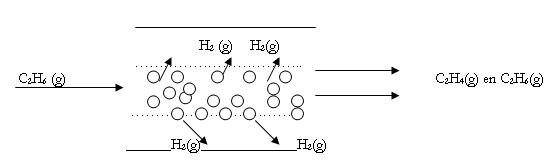 |
| Afbeelding 5 |
Opgave 12
a.
Welke scheidingsmethode had men moeten toepassen wanneer het waterstofgas niet via het membraan was afgescheiden. Leg uit. b. Is de opmerking dat er veel energie wordt bespaard terecht? Licht toe.
5. Massabalans en energiebalans
Bij ieder proces geldt de wet van massabehoud. De massa van alle stoffen samen die de reactor ingaan is gelijk aan de massa van alle stoffen samen die uit de reactor komen.
Voor ieder element apart geldt natuurlijk ook de wet van massabehoud.
Bij het ontwerpen en doorrekenen van een chemische fabriek gebruikt een proces ingenieur deze wet. Men noemt dit de massabalans van een proces.
Zo kan men ook een energiebalans opmaken voor een proces, omdat de wet van energiebehoud ook opgaat.
Opgave 13
Bij het continu proces bij de reactie tussen etheen en water tot ethanol. blijkt bij ieder doorgang van het reactiemengsel door de reactor slechts 5,0 % van het etheen te worden omgezet. Maar door etheen terug te winnen en te recirculeren, wordt er uiteindelijk ruim 99, 5 % van omgezet.
Uit de reactievergelijking blijkt dat etheen en stoom in de verhouding 1:1 reageren.
Men gebruikt toch een ondermaat waterdamp, omdat bij teveel water de katalysator teveel oplost in het water. Men voegt etheen en waterdamp bijeen in de verhouding 1: 0,6.
a.
Stel dat er 40 mol ethanol per uur wordt gevormd. Bereken hoeveel mol etheen per uur via de recirculatielus terug wordt gebracht in de reactor. b. Bereken hoeveel mol waterdamp per uur via de recirculatielus terug wordt gebracht in de reactor. c. Bereken hoeveel mol etheen nieuw moet worden toegevoegd per uur.Ga er hierbij vanuit dat alle mogelijke etheen en waterdamp ook worden teruggewonnen. d. Bereken hoeveel mol waterdamp nieuw moet worden toegevoegd per uur.
Overzichtsopgaven over proceschemie.
Opgave 14
Shampoos bevatten zogenoemde synthetische zepen. Een voorbeeld van een (synthetische) zeep die in shampoos voorkomt, is natriumlaurylsulfaat (C12H25OSO3-Na+).
Laurylwaterstofsulfaat wordt bereid uitgaande van laurylalcohol (C12H25OH). Alcoholen met 10 of meer C atomen per molecuul, zoals laurylalcohol, worden vetalcoholen genoemd. Vetalcoholen kan men bereiden uitgaande van bijvoorbeeld kokosolie. Kokosolie bestaat uit glyceryltri esters van carbonzuren die ongeveer 12 C atomen per molecuul bevatten. Een voorbeeld van zo'n glyceryltri-ester is:
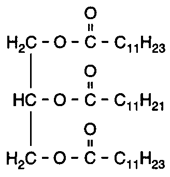
De industriële bereiding van vetalcoholen is een continu proces dat als volgt in een (nog onvolledig) blokschema 1 kan worden weergegeven:
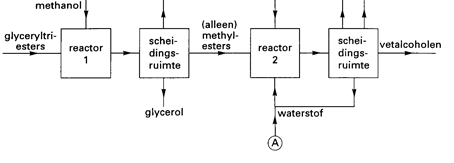
Blokschema 1
In reactor 1 reageren de glyceryltri esters met methanol dat in overmaat wordt toegevoerd:
glyceryltri esters + methanol → methylesters + glycerol
In reactor 2 reageren de gevormde methylesters met waterstof die in overmaat wordt toegevoerd. Een voorbeeld van een reactie die daarbij optreedt, is:
![]()
In reactor 2 ontstaan ook kleine hoeveelheden van zogenoemde wasesters. Een voorbeeld van zo'n wasester is:
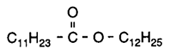
De ontstane wasesters worden na afscheiding teruggeleid naar reactor 2 waar ze worden omgezet in vetalcoholen. Het hele, continue proces kan als volgt schematisch worden weergegeven:
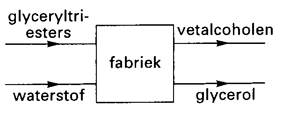
Mede met behulp van dit schema is af te leiden dat het eerder gegeven blokschema 1 niet compleet is: niet alle lijnen die de stofstromen weergeven, staan erin. Op de bijlage staat het niet complete blokschema weergegeven.
Maak het blokschema 1 compleet door het plaatsen van lijnen. Zet bij de nieuwe lijnen ook bijschriften.
Opgave 15
Een totaal andere manier om ethanol te produceren is om vanuit een plant zoals suikerriet, suikerbiet, aardappel e.d. te beginnen.
Wanneer de plant maar voldoende suikers bevat is het mogelijk om ethanol te synthetiseren.
De volgende stappen vinden plaats bij deze synthese:
- Complexe suikers worden afgebroken tot eenvoudige suikers, zoals glucose en fructose.
- Bij ca. 35 °C wordt gist toegevoegd en na enkele dagen is er een maximum haalbare hoeveelheid (max. 15 %) ethanol gevormd. Bij de gisting worden de suikers omgezet in koolstofdioxide en ethanol.
- Het ethanol moet worden gewonnen uit het reactiemengsel.
a. Teken met behulp van bovenstaande gegevens het blokschema voor dit proces.
In de volgende tabel staan een aantal belangrijke punten voor beide processen genoemd.
| Gisting | Additiereactie | |
| Soort proces | Batchproces | Continu proces |
| Reactiesnelheid | Langzaam | Snel |
| Kwaliteit van het product | Zeer onzuiver ethanol | Vrij zuiver ethanol |
| Reactie omstandigheden | Lage temperatuur; standaarddruk | Hoge temperatuur; hoge druk; katalysator |
| Grondstoffen | Hernieuwbare grondstoffen op basis van planten | Niet-hernieuwbare grondstoffen, die afkomstig zijn uit aardolie |
b.
Beredeneer met behulp van chemische argumenten op grond van de gegevens in maximaal 100 woorden welk proces jouw voorkeur heeft. c. Leg uit of je tot dezelfde conclusie komt wanneer je let op de principes van de duurzame chemie.
Opgave 10
ZEPPen VOOR HET MILIEU!
ZEPP is een van de mogelijke manieren om zonder schadelijke emissies elektriciteit op te wekken.
a.
Waar staat de afkorting ZEPP voor? b. Welke brandstoffen kunnen in een ZEPP-centrale toegepast worden? c. Aan welke eisen moet de brandstof minimaal voldoen?
Men gebruikt bij de verbranding zuivere zuurstof.
d. Hoe kan men uit lucht zuivere zuurstof halen?
Men injecteert water in de hete verbrandingsgassen.
De centrale produceert als afval alleen koolstofdioxide en water.
e.
Leg uit dat daardoor de temperatuur van de verbrandingsgassen daalt. f. Leg uit dat de hete stoom die daarbij ontstaat een turbine in werking kan zetten. g. Hoe verloopt de vorming van elektriciteit verder?
Jaarlijks produceert men 275 kiloton koolstofdioxide.
h.
Geef de reactievergelijking van de verbranding van methaan in de ZEPP-centrale. i. Waarom zal men in een ZEPP-centrale zuivere zuurstof gebruiken en geen lucht?
De tekening in het artikel kun je vertalen naar een blokschema.
j. Bereken hoeveel kg methaan er dan verbrand is. Gegeven: 1 ton = 1000 kg.
k.
Maak een compleet blokschema van de ZEPP. l. Op welke wijze draagt deze electriciteitscentrale bij aan de principes van de groene chemie? m. Bedenk een aantal punten in het proces waar nog winst is te behalen. Licht toe.
 |
| Technisch Weekblad, 23 September 2005 |
Bron: Chemie Aktueel, nr 51