Antibiotica (5h) - Docentenhandleiding
U kunt het leerlingenmateriaal van de module voor 5 havo ook in z'n geheel downloaden als pdf-bestand. Voor 5 havo is gekozen voor de thema’s ‘Groene Chemie’ en ‘Synthese’. De module krijgt een plek in de groene leerlijn (havo) van het Examenexperiment Nieuwe Scheikunde. De module kan het best gegeven worden in de periode september/november. De module “Groene chemie” kan goed voorafgaand aan de module “Antibiotica” gegeven worden. |
| |
| 1. Korte beschrijving van de inhoud van de module |
| 2. Schematisch overzicht van de module |
| 3. Kenniskaarten: wat zijn dat? |
| 4. Beschrijving van de lessen |
| 5. Voorbeeldproefopgaven |
| Bijlage: Welke domeinen en concepten komen in de module ‘Antibiotica’ aan de orde? |
| Bijlage: Overzicht van relaties/mogelijkheden van de module ‘Antibiotica’ |
| Bijlage: Veiligheidsinformatie 6-APA |
| Bijlage: Veiligheidsinformatie HPGM |
| Bijlage: Veiligheidsinformatie Assemblage liquid |
| Bijlage: TOA-tips |
1. Korte omschrijving van de inhoud van de module
Allereerst activeren we de voorkennis op het gebied van antibiotica en introduceren we de contextvragen:
| Wordt het antibioticum van de toekomst gemaakt door de mens of door een micro-organisme? | |
| En: | Hoe kunnen leerlingen uit 5 havo een bijdrage leveren aan de ontwikkeling van een antibioticum? |
Vervolgens laten we leerlingen op een simpele manier bacteriën opkweken. Het effect van antibiotica op bacteriegroei komt aan de orde. In het verloop van de module zoomen we steeds verder in op de moleculaire achtergronden. We bespreken de moleculaire bouw van de bacteriecelwand. Op een vereenvoudigde manier laten we zien hoe penicilline aangrijpt op de bacteriecelwand.
Bacteriecelwanden zijn opgebouwd uit gemodificeerde koolhydraatketens die onderling verbonden zijn door kleine stukjes eiwit. Daarom wordt in de module ook beknopt aandacht gegeven aan koolhydraten. Aminozuren en eiwitten - en de daarbij horende peptidebinding - worden uitvoeriger besproken.
In ons lichaam vinden duizenden reacties plaats onder milde omstandigheden. De ene keer worden moleculaire bouwstenen onderling gekoppeld. Bijvoorbeeld bij de vorming van een eiwit. Een volgende keer worden grote moleculen in kleinere eenheden geknipt. Steeds zijn daarbij enzymen betrokken. Daarom besteden we in de module aandacht aan de functie en werking van enzymen.
In de industrie gaat men steeds vaker over op enzymatische omzettingen om moleculen om te zetten of om moleculen te knippen. Leerlingen voeren de laatste synthesestap uit van de omzetting van penicilline G in amoxicilline. Het aardige hiervan is dat de tussenproducten (PAA en 6-APA) niet werken als antibioticum, maar amoxicilline wel.
We gaan in op de vraag waarom men in de industrie steeds vaker overstapt op enzymatische omzettingen. En we gaan in op de vraag hoe men in de industrie aan enzymen komt om syntheses te doen.
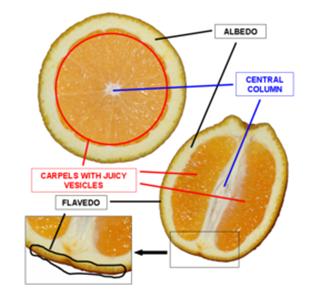
Hier komt het eigen onderzoek van de leerlingen in beeld. We ondernemen samen met de leerlingen een speurtocht naar nieuwe enzymen. We maken daarbij uiteraard gebruik van de natuurwetenschappelijke methode. Samen met medewerkers van DSM en de VU zijn we op zoek gegaan naar een aantal ‘huis-tuin-en-keuken-enzymen’. Om een zo groot mogelijke kans op succes te hebben gaan we op zoek naar een ‘fosfatase’. Fosfatases splitsen een fosfaat-groep van een organisch molecuul af. Voor deze omzetting bestaat een eenvoudige testreactie. De fosfatase kan bijvoorbeeld vrij gemakkelijk gevonden worden in fruit.
Dit is het spannendste gedeelte van de module! (Trouwens ook tijdens het ontwikkelen van de module).In de afsluitende les kijken we terug op het onderzoek. Ook kijken we vooruit. We gaan daarbij in op één van de nieuwste ontwikkelingen binnen de natuurwetenschap: de ‘synthetische biologie’.
Tot slot formuleren de leerlingen hun antwoord op de contextvragen.
Soort les: | |
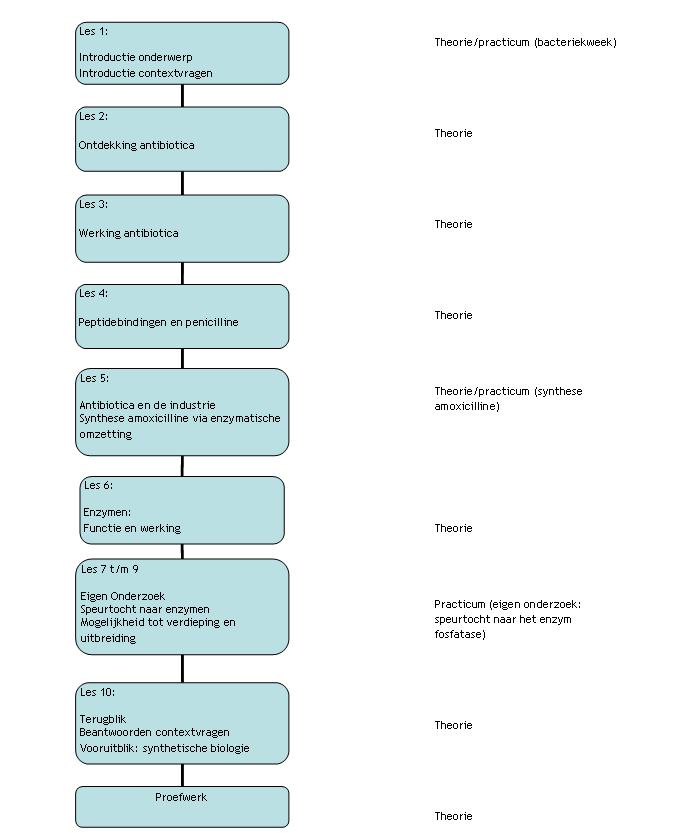 | |
3. Kenniskaarten: wat zijn het?
De lastigste leerstofonderdelen zijn apart beschreven in zogenaamde kenniskaarten. Een leerling die de inhoud van de kenniskaarten leert moet in staat zijn om het proefwerk over de modulestof te maken. Kenniskaarten zijn dus bedoeld als ondersteuning van het modulemateriaal. Er zijn kenniskaarten beschikbaar over:
Kenniskaart | soort informatie | hoort bij les |
| 1. Micro-organismen | voorkennis, leerstof | 1 en 3 |
| 2. Antibiotica | leerstof | 1 en 2 |
| 3. Penicilline | leerstof | 2 en 3 |
| 4. Onderzoek, hoe doe je dat? | leerstof | 2 en 7 t/m 9 |
| 5. Structuurformules | voorkennis, leerstof | 4 |
| 6. Naamgeving organische chemie | voorkennis, leerstof | 4 |
| 7. Eigenschappen van alkanolen, alkaanzuren, alkaanaminen en aminozuren | leerstof | 4 |
| 8. Condensatiereacties | leerstof | 4 |
| 9. Enzymen | leerstof | 3 en 6 |
| 10. Reactiesnelheid | leerstof | 6 |
| 11. Responsible Care | informatie | 1 t/m 6 |
| Les 1: | In deze les halen we de voorkennis op. Leerlingen moeten een mindmap ontwerpen.
| ||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| Les 2: | De ontdekking en ontwikkeling van antibiotica komen aan de orde. De Natuurwetenschappelijke methode wordt beknopt besproken. Ook gaan we voor het eerst in op de structuurformules van de belangrijkste antibiotica, namelijk penicilline G en daarvan afgeleid amoxicilline. | ||||||||||||||||||||||||||||||||||
| Les 3: | De werking van antibiotica staat centraal. We zoomen steeds verder in. We starten met een schematisch overzicht van de bouw van een bacteriecelwand. Uiteindelijk komen we uit bij de moleculaire bouwstenen, zoals aminozuren. De werking van penicilline komt op een vereenvoudigde wijze aan de orde. Leerlingen zullen de theorie als pittig ervaren. Door de stapsgewijze aanpak denken we dat ze zich de theorie eigen kunnen maken. Wilt u precies weten hoe het zit kijk dan eens bij: http://www.scq.ubc.ca/prescription-antibiotics-how-exactly-do-these-drugs-work/ | ||||||||||||||||||||||||||||||||||
| Les 4: | De vorming van eiwitten vanuit aminozuren wordt besproken. Aminozuren, eiwitten en peptidebinding komen aan de orde. Ook gaan we in op de hydrolyse van eiwitten. Steeds weer komen we terug op de context. Hoe zit het met de eiwitbrug in de celwand van een bacterie? Hoe kan het dat penicillinemoleculen kapot gaan voordat ze hun werk gedaan hebben? Steeds geldt dat we de werkelijkheid zo nauwkeurig mogelijk volgen. Omdat de moleculaire werkelijkheid vaak toch nog weer complexer is hebben we vereenvoudigingen toegepast. | ||||||||||||||||||||||||||||||||||
| Les 5: | Centraal staat de synthese van Amoxicilline zoals DSM die uitvoert. Ook is er aandacht voor het verschil tussen organische syntheses en enzymatische omzettingen. Leerlingen voeren zelf de laatste, enzymatische, stap uit van de omzetting van penicilline G naar Amoxicilline. Chemicaliën, zoals (6-APA en HPGM), zijn beschikbaar. Stuur – op tijd(!) - een mail naar: info@scheikundeinbedrijf.nl U ontvangt dan z.s.m. informatie over de manier waarop de beginstoffen te verkrijgen zijn. Let op: ook voor het onderzoek dat de leerlingen tijdens de lessen 7 t/m 9 doen zijn chemicaliën beschikbaar.
| ||||||||||||||||||||||||||||||||||
| Les 6: | De functie en werking van enzymen wordt uitgediept. Reactie-energie, activeringsenergie en het effect van een enzym komen aan de orde. In de module Scooter is al aandacht gegeven aan ‘actief complex’. Daarop kan eventueel worden teruggegrepen. Er is aandacht voor de vraag hoe bedrijven aan enzymen komen. En hoe ze oplossingen testen op enzymactiviteit. In deze les krijgen de leerlingen een aantal voorbeelden van enzymreacties, o.a. een peptidase, een protease en een fosfatase. Prachtig achtergrondmateriaal over enzymen is te vinden op: http://www.vib.be/InfoEdu/Nl/Educatief+materiaal/. Op deze site staan uitstekend leesbare brochures, bijvoorbeeld: “Enzymen: in je lijf en in je leven.” | ||||||||||||||||||||||||||||||||||
| Les 7 t/m 9: | In deze lessenserie gaan leerlingen zelf op zoek naar een enzymbron met hopelijk(!) daarin een werkzame fosfatase. In verband met dit eigen onderzoek komen we terug op de Natuurwetenschappelijke methode, die in les 2 ook al aan de orde kwam. Leerlingen onderzoeken hun enzymbron met behulp van een testreactie. Ook hiervoor geldt dat de benodigde chemicaliën beschikbaar zijn. Stuur een mail naar: info@scheikundeinbedrijf.nl. Het artikel dat als bron is gebruikt voor het experiment is te vinden op de site: De bronnen die in het artikel gebruikt worden zijn het vruchtvlees en (verschillende lagen van) de schil van grapefruits en sinaasappelen. Uit onze tests is gebleken dat met name de schil van een grapefruit een uitstekende bron van fosfatase is. In de (positieve) test die wij hebben gebruikt hebben we de volgende monsters getest: Van de filtraten werd steeds 2 mL gemengd met 5 mL teststock. Na 15 minuten was er al een duidelijk meetbaar effect als 0,5 mL van het mengsel werd toegevoegd aan de 20 mL carbonaatbuffer. De meting gebeurde in een UV-spectrofotometer bij 440 nm. De resultaten waren als volgt:
In de testfase van de module is deze opdracht o.a. uitgevoerd tijdens een projectdag. Na een introductie over het doen van onderzoek en de wijze van verslaglegging hebben leerlingen tussen 9.30u en 14.00u hun onderzoek uitgevoerd en een verslag geschreven. Ze hadden zelf fruit en groenten meegenomen. Daarbij zaten o.a. kokosnoten (die nog fosfatase bleken te bevatten ook)! Op school waren nog extra groenten en fruit aanwezig. Leerlingen hadden zelf ook mixers bij zich. Dat was nodig omdat er 75 leerlingen tegelijkertijd het onderzoek uitvoerden. Op school waren te weinig blenders voorhanden. Leerlingen vonden het onderzoek heel goed te doen en tegelijkertijd heel spannend omdat ze heel benieuwd waren of hun fruit/groente fosfatase bevatte. Over eigenaarschap gesproken! In 5 VWO diende deze ‘onderzoeksprojectdag’ meteen ook als start voor het profielwerkstuk. Les 7 t/m les 9 verdieping: Door op regelmatige tijden monsters te nemen kan ook de snelheid van omzetting gemeten worden als maat voor de (kinetische) activiteit van het fosfatase.
Les 7 t/m les 9 verdieping vervolg:5 vwo leerlingen zouden ook zelf aan de buffer-oplossingen kunnen rekenen: | ||||||||||||||||||||||||||||||||||
| Les 10: | In laatste les komen de contextvragen terug. | ||||||||||||||||||||||||||||||||||
5. Voorbeeldproefwerkopgaven
Voorbeeldtoetsvragen zijn te vinden op het docentenforum van mijnscheikunde.nl. Om toegang te krijgen tot het forum dient u zich eenmalig te registeren. Hier zijn geen kosten aan verbonden. Voor aanvullende vragen kunt u mailen naar info@scheikundeinbedrijf.nl